Inscription / Connexion Nouveau Sujet
Rendement
Bonsoir, j'ai un problème sur un exercice que je dois rendre lundi.
Malgré plusieurs essais je n'ai toujours pas trouvé la solution.
Voici l'énoncé:
On chauffe à reflux pendant trente minutes un mélange constitué d'un volume V(ol)=30.0 mL de 3,3diméthylbutan-1-ol et de 5 mL d'acide sulfurique concentré. On obtient un alcène.
Le mélange alors obtenu est introduit dans une ampoule à décanter. La phase aqueuse est éliminée : la phase organique est lavée, puis séchée par du sulfate anhydre.Après filtration, on obtient une masse m'=11.6g d'alcène
données: Densité de l'alcool : d(ol)=0.812
Masse volumique de l'eau : 1.00 g.mol-1
L'alcène est insoluble dans l'eau, sa densité est inférieure à 1.
Masse molaires atomiques : h=1 c=12 o=16
Je dois calculer le rendement de cette synthèse.
Je sais qu'il me faut le n final et le n initial mais pas moyen de trouver.
J'ai aussi calculé la masse molaire de l'alcool et j'ai obtenu 102g.mol
Pouvez vous m'aider ? Merci
écris l'équation de réaction.
on aura alcool + (H+ ) = alcène + eau
j'ai mis H+ entre parenthèses car c'est un catalyseur.
m(alcool)=V* 
n(alcool)=m/M
si la réaction était totale on obtiendrait n (alcène)=n(alcool)
la qté réellement obtenue est n(réelle)=m(réelle)/M(alcène)
le rendement est
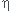 = n(alcène réellement obtenue)/n(alcène)max
= n(alcène réellement obtenue)/n(alcène)max
pour avoir la formule brute de l'alcène ,il suffit de retirer H2O à la formule de l'alcool.
de ce fait M(alcène)= M(alcool)-M(H2O)
pour avoir la formule développée de l'alcène tu supprimes OH du carbone 1 ,tu supprimes H du carbone 2 et tu écris une double liaison entre C1 et C2
Alors ,
M(alcène) = 102- M(h2O)
= 102-18
= 84g.mol
m alcène = 11.6g
Donc : n alcène = 11.6/84  0.14
0.14
m(alcool) = 30*1
= 30
M(alcool) = 102g.mol
Donc : n alcool = 30/102  0.29
0.29
Rendement = 0.14/0.29  0.48
0.48
Donc rendement à 48 % ?
donc en changeant :
m(alcool) = 30*0.812 = 24.36
donc n = 24.36/102 0.24
0.24
Rendement= 0.14/.024=0.58 donc 58%
Et là c'est correct ?


