Inscription / Connexion Nouveau Sujet
Dosage acido-basique. explications
Bonjour à tous
Voici ma courbe (en pièce jointe) associé à ce texte :
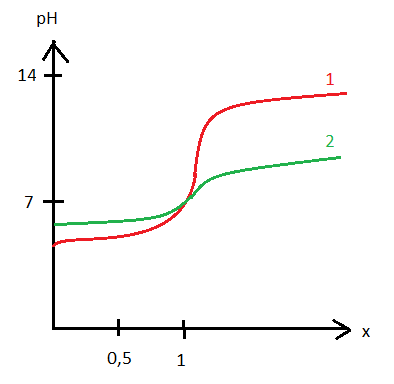
On réalise le dosage d'un acide par une base forte. On trace la courbe de dosage pH = f(x), où x représente la fraction d'acide salifié, pour deux concentrations différentes de l'acide. On obtient les courbes 1 et 2.
On me dit que ces deux phrases sont fausses :
1) Il s'agit d'un acide fort car on n'a pas pH=pKa pour les deux courbes
2) Le pH = 7 à l'équivalence justifie le dosage d'un acide fort dans les deux cas.
On me dis que ces deux phrases sont vraies :
3) La relation pH=pKa à la demi équivalence ne s'applique pas aux solutions trop diluées.
4) L'acide se comporte comme un acide fort dans le cas de la courbe 2.
Je n'ai aucune explication de ces phrases.
J'arrive à en trouver une pour la 4) : nous voyons que la courbe 2 du pH évolue faiblement vers un état basique. L'acide se comporte donc comme un acide fort.
Pouvez vous me donner plus d'explications pour : 1) 2) 3) et 4) ?
Merci.
Salut,
la courbe 1 est la courbe caractéristique d'un dosage d'un acide faible par une base forte
la courbe 2 est la courbe caractéristique d'un dosage d'un acide fort par une base forte
on le voit notamment au début de la courbe, il est droit pour l'acide fort, il est courbé pour l'acide faible.
donc
phrase 1 fausse car la courbe 2 on a pH=pKa
phrase 2 fausse car la courbe 2 n'a pas l'équivalence pour pH=7
phrase 3 vraie car effectivement les courbes ne se rencontrent pas à la 1/2 équivalence.
phrase 4 vraie car effectivement l'acide faible dilué à une courbe d'acide fort (courbe 2)


