Inscription / Connexion Nouveau Sujet
Spectre de l'atome d'hydrogène et les photons
Bonjour, j'ai un exercice de physique à faire sur lequel je bloque particulièrement 
J'ai pourtant bien réussi le reste, mais cet exercice de synthèse, je n'y arrive pas.
Voici l'énoncé :
1) a) Dans le spectre d'émission de l'atome d'hydrogène, retrouve-t-on les raies correspondant aux photons émis lorsqu'un atome d'hydrogène dans un état excité retourne à l'état fondamental ?
Justifier votre réponse.
b) Quelle est l'énergie d'un photon de la raie rouge ? ( =656 nm) du spectre d'émission de l'hydrogène ? Cette énergie correspond-elle à la différence d'énergie entre deux états d'un atome d'hydrogène ?
=656 nm) du spectre d'émission de l'hydrogène ? Cette énergie correspond-elle à la différence d'énergie entre deux états d'un atome d'hydrogène ?
Si oui, préciser ces états et conclure.
c) A quels changements d'état correspondent les raies cyan ( =486 nm) et bleue (
=486 nm) et bleue ( =434 nm) du spectre de l'hydrogène ?
=434 nm) du spectre de l'hydrogène ?
2) Comment peut-on justifier qu'une entité chimique possède un spectre de raies d'émission spécifique ?
Merci d'avance 
ps : Voici le spectre en question :
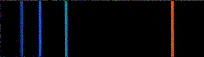
oui car lors de sa transition d'un niveau plus haut en énergie vers un niveau plus bas on parle d'absorbtion de photons. Les raies d'émission et les raies d'absorbtion sont complémentaire
sauf que pour que le spèctre d'absorbtion sera des raies noir sur fond de couleurs
b:  E=h
E=h c/
c/ 
h(constante de Planck)=6,63 10^-34
10^-34
c(la célérité)=3 10^8
10^8
 =656 nm
=656 nm
attention l'énergie s'exprime en eV
désolé c'est pas ca 
b:  E=hc/
E=hc/
h(constante de Planck)=6,63 10^-34m2.kg.s-1
10^-34m2.kg.s-1
c(la célérité)=3,00 10^8m.s-1
10^8m.s-1
 =656 nm
=656 nm
attention LA LONGEUR D'ONDE S'exprime en METRE
donc tu doit multiplier 656 par 10^-9
L'énergie s'exprime en JOULE
Ce qui te fait: 3.02 10^-19 J
10^-19 J
pour le b) ce que mirab a dit est bon mais pour répondre à la fin de la question b) tu dois convertir en électron-volt, c'est-à-dire diviser 3.02*10^-19 par 1.60*10^-19
donc 3.02*10^-19/1.60*10^-19=1.89eV
et pour la suite du b) tu peut dire que cette énergie correspond à la transition d'énergie entre l'état E3 et l'état E2 d'un atome d'hydrogène car  E= Ep-En ce qui fait
E= Ep-En ce qui fait
 E= -1,51-(-3.4)
E= -1,51-(-3.4)
 E= -1,51+3.4
E= -1,51+3.4
 E= 1.89 eV
E= 1.89 eV


