Inscription / Connexion Nouveau Sujet
déterminer le nombre de doublets non-liants d'une molécule
bonjour! Pouvez-vous m'expliquer comment déterminer le nombre de doublets non-liants d'une molécule en ne conaissant que sa structure électronique?
Je doit trouver le nombre de doublets non-liants de la molécule C2H6O 
Bonjour,
Je te copie le message que j'ai écris il y a quelques jours :
Bonsoir,
Il faut que tu écrives la configuration électronique de l'atome avec le remplissage des couches (K), (L) et (M).
Prenons deux exemples :
(a) L'atome de carbone : Z=6 d'où la configuration électronique suivante (K)2(L)4. Tous les atomes tendent à obtenir la configuration la plus stable possible, c'est-à-dire en duet ou en octet.
Ici, il faut gagner quatre électrons pour avoir une structure en octet. En effet, la couche (L) peut contenir jusqu'à huit électrons, il en faut donc quatre de plus pour qu'elle soit entièrement remplie.
Le carbone engage donc quatre liaisons, ce sont les doublets liants.
Pour calculer le nombre de doublets non-liants, il faut calculer la différence entre le nombre d'électrons sur la couche externe et le nombre d'électrons engagés dans un doublet liant. Ici, on a 4-4=0 donc aucun doublet non liant.
(b) L'atome d'oxygène : Z=16 d'où la configuration électronique suivante (K)2(L)8(M)6.
Pour obtenir une structure en octet, il faut que l'oxygène gagne deux électrons pour saturer la couche (M). Il engage donc une seule double liaison.
Il reste donc 6-4=2 électrons sur sa couche externe, d'où un seul doublet liant.
Et voilà
Pour voir si tu as bien compris la méthode, essaye avec de l'appliquer sur l'exemple de l'azote (Z=7) et je te dirais si c'est correct.
Merci beaucoup! 
Donc si on a l'atome d'azote avec z=7, sa structure électronique est égale à K2L7
et il doit engager 3 laisons pour satisfaire la règle de l'octet.
Il reste donc 7-3=4 électrons sur sa couche externe, soit 2 doublets liants.
Es-ce-que c'est juste? Merci en tout cas pour votre aide!
Oui, Z=7 donc il y a sept électrons à placer. On commence par remplir (K) qui peut continuer 2 électrons puis (L), si besoin, qui peut contenir 8 électrons puis (M), si besoin, qui peut contenir 8 électrons.
ok, donc l'atome d'azote doit engager une liaison et 7-1=6, il possede donc 3 doublets non-liants et uen doublet liant.  right?
right?
Pourquoi ? Sa structure électronique est (K)2(L)5 donc, pour satisfaire à la règle de l'octet, il doit engager 3 liaisons (il y a 5 électrons sur la couche externe et il faudrait en avoir 8 pour satisfaire à cette règle).
Il reste donc 5-3=2 électrons soit un doublet non-liant.
De rien 
Comme tu as eu un peu de mal avec l'azote, je te donne un autre exemple pour être sûr que tu aies bien compris la méthode : essaye avec l'atome de chlore (Z=17).
ok alors,la structure électronique de l'atome de chlore est K2L8M7 et 8-7= 1, donc l'atome Cl doit engager 1 liaison.
7-1= 6, il possède donc 3 doublets non-liants! 
Es-ce-que tu pourrais me dire si ce que j'ai fait est bon? :
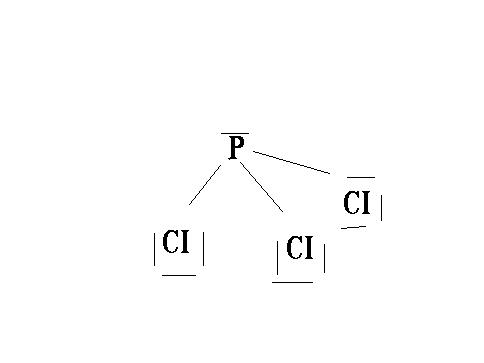
Soit la molécule PCI3, les stucture électronique des atome P et Cl sont:
p= K2L8M5 et Cl=K2L8M7
l'atome de phosphore doit donc engager 5 liaisons et l'atome de chlore doit en engager 3.
l'atome de phosphore possede donc 5-5=0 doublets non liants et l'atome de chlore possede 7-3=4, soit 2 doublets non liants.
La molécule PCI3 possede en tout 5+3*3=14 électrons contenus dans les doublets liants, soit 14/2= 7 doublets liants.
Merci d'avance! 
Non...
Combien d'électrons manque-t-il au phosphore pour acquérir une structure en octet ? (pas 5 en tout cas...)
Combien d'électrons manque-t-il au chlore pour acquérir une structure en octet ? (pas 3 en tout cas...) En plus, tu as traité l'exemple du chlore un message plus haut...
j'ai confondu....alors l'atome de phosphore doit engager 3 liaisons et l'atome de chlore doit en engager 1.
5-3=2: l'atome de phosphore aura donc un doublet non-liant
7-1= 6: l'atome de chlore aura donc 3 doublet non-liant
la molécule PCl3 possède en tout 6+3*2=12 électrons dans l'ensemble de ses doublets liants
soir 12/2= 6; la molécule PCI3 est donc constituée de 6 doublets liants!
Attention, à la 4ème ligne : "dans l'ensemble de ses doublets NON-liants".
Sinon, le reste est juste : PCl3 possède donc 10 doublets non-liants et 6 doublets liants.
Oui c'est ça 
D'ailleurs on avait dit une bêtise : il n'y a pas 6 doublets liants mais uniquement 3 (on les a comptés deux fois).
Bonjour masterrr,
Je suis une élève de première et je trouvais que vos explications étaient particulièrement intéressante cependant,je ne suis pas du tout sûre, mais je crois que vous vous êtes trompez à : ( au numéro atomique plus précisément )
" (b)L'atome d'oxygène : Z=16 d'où la configuration électronique suivante (K)2(L)8(M)6.
Pour obtenir une structure en octet, il faut que l'oxygène gagne deux électrons pour saturer la couche (M). Il engage donc une seule double liaison.
Il reste donc 6-4=2 électrons sur sa couche externe, d'où un seul doublet liant. "
Car Z=8 pour O et non 16, le nombre 16 est le numéro de la colonne et aussi dans ce cas la masse molaire atomique.
Du coup, votre démonstration est fausse.
Bonne journée,
J'espère avoir une réponse rapide de votre part 
Aure1909.