Inscription / Connexion Nouveau Sujet
Titrage du vinaigre
Protocole expérimental
On dispose d'une solution (S1) obtenue en diluant 10 fois du vinaigre commercial. En introduire exactement 10,0 mL dans un bécher. Ajouter environ 20mL d'eau distillée.
Rincer la burette avec quelques millilitres de soude (CB = 0,100 mol.L-1), puis la remplir en vérifiant qu'il n'y a pas de bulle d'air coincée au niveau du robinet, ajuster le niveau "0".
Etalonner le pH-mètre puis rincer et sécher l'électrode.
Mesurer le pH de la solution.
Ajouter un des indicateurs colorés mentionnés dans le tableau ci-dessous. Chaque binôme choisira un indicateur différent.
Ajouter, à la burette, 2 mL la solution titrante ; mesurer le pH et noter sa valeur.
Ajouter, mL par mL, 20 mL de solution titrante en relevant les valeurs du pH, le volume VB de soude ajoutée et la couleur de la solution. Reportées les données expérimentales dans un tableau à trois colonne : VB, pH, couleur de la solution.
Exploitation
Tracer la courbe représentant l'évolution du pH en fonction du volume de soude versée : pH=f(VB)
Détermination du point d'équivalence par la méthode des tangentes
Choisir de part et d'autre du point d'inflexion deux points de la courbe dans les domaines de forte concavité tels que les tangentes à la courbe en ces points soient parallèles
Une troisième parallèle équidistante aux deux tangentes coupe la courbe au point d'équivalence E.
Donner les coordonnées du point d'équivalence (VBeq, pHeq).
J'ai trouvé pour le point E : VB = 13.5 mL et pH = 8.25
Écrire la demi-équation de chacun des couples acide/bases impliqués et l'équation de la réaction du titrage. (FAIT)
A l'aide d'un tableau d'avancement, établir la relation entre la quantité de matière d'acide éthanoïque initialement présente et celle de soude versée à l'équivalence. (FAIT)
En déduire la concentration précise en acide éthanoïque dans le vinaigre dilué (S1) puis dans le vinaigre commercial.
(Je ne comprends pas comment trouver la concentration du vinaigre commercial, mais j'ai trouvé la concentration de S)
Rappel: le degré d'acidité d'un vinaigre est la masse en grammes d'acide acétique pur contenu dans 100 g de ce vinaigre.
Vérifier le degré d'acidité du vinaigre sachant que sa masse volumique est = 1,02 g.cm-3.
Je ne sais pas comment faire
Bonjour,
Si tu as le concentration de la solution S tu peux retrouver la concentration du vinaigre commercial vu qu'il a été dilué 10 fois...
Salut,
soit la solution (S) de vinaigre commercial de concentration C
La solution fille (S1) utilisée pour le dosage a
* un volume Va
* une concentration Ca = C/10 (10 fois diluée)
La solution titrante est la soude (Na+ + OH-) avec
* Cb la concentration de cette solution
* Vbe = volume versé de soude à l'équivalence
__________________________________________________________________________________________________
Schéma du dispositif :
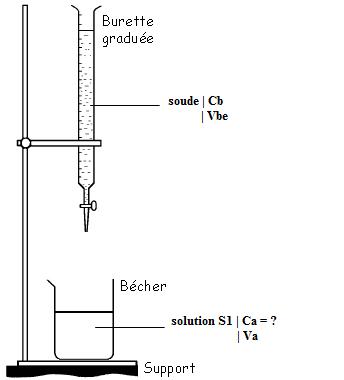
L'équation de la réaction du dosage est CH3COOH + HO- = CH3COO- + H20
L'équivalence est atteinte quand les réactifs de la réaction du dosage ont été introduits dans des proportions stoechiométriques.
Donc à l'équivalence,
<=> Ca.Va = Cb.Vbe
donc
Application numérique à faire : Ca = ....... mol/L
Finalement, la concentration de la solution commerciale est C = 10.Ca = .... mol/L




